Kuidas elektrisõiduki liitiumioonaku töötab?
Olles näinud teises artiklis pliiaku tööd, millega kõik autod on varustatud, vaatame nüüd elektrisõiduki ja eriti selle liitiumaku tööpõhimõtet ...

Prints
Nagu igat tüüpi akudel, jääb põhimõte samaks: nimelt toota energiat (siinkohal elektrit) keemilise või isegi elektrilise reaktsiooni tulemusena, sest keemia on alati elektri kõrval. Tegelikult on aatomid ise valmistatud elektrist: need on elektronid, mis tiirlevad ümber tuuma ja mis mingil moel moodustavad aatomi "kesta" või isegi selle "naha". Teades ka seda, et vabad elektronid on lendlevad nahatükid, mis veedavad oma aega ühest aatomist teise liikudes (ilma sellega kinnitumata), on see ainult juhtivate materjalide puhul (sõltub elektronide kihtide arvust ja elektronide arvust). viimase mürsu kohta).
Seejärel võtame aatomitelt "nahatüki" (seega osa selle elektrist) keemilise reaktsiooni kaudu elektri tootmiseks.

põhitõed
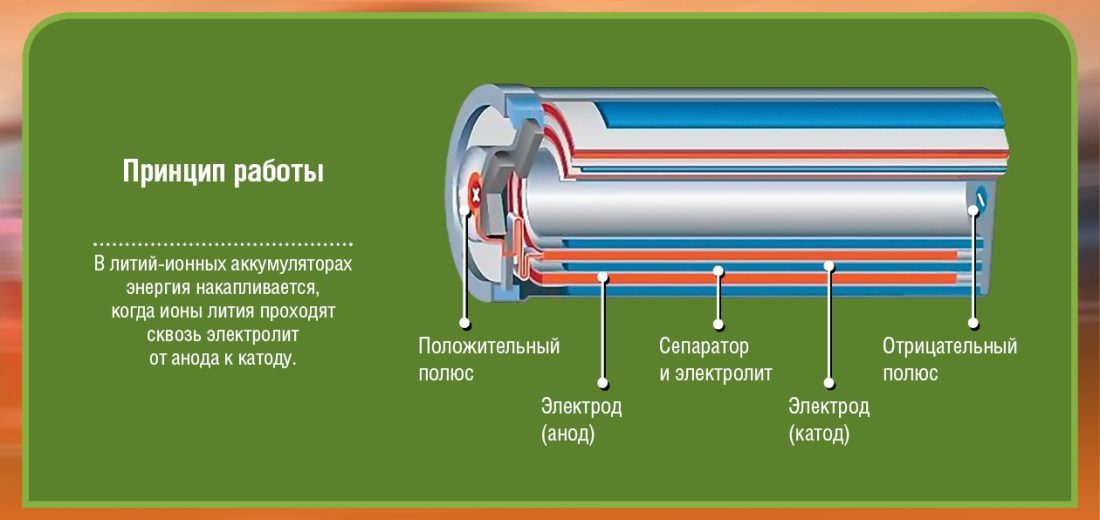
Esiteks on kaks poolust (elektroodi), mida me nimetame katood (+ klemm: liitium-koobaltoksiidis) ja anood (terminal -: süsinik). Kõik need poolused on valmistatud materjalist, mis kas tõrjub elektrone (-) või tõmbab ligi (+). Kõik on üle ujutatud elektrolüüt mis teeb võimalikuks keemilise reaktsiooni (materjali ülekandumise anoodilt katoodile) elektrienergia tootmise tulemusena. Nende kahe elektroodi (anood ja katood) vahele sisestatakse barjäär, et vältida lühiseid.
Pange tähele, et aku koosneb mitmest elemendist, millest igaüks koosneb diagrammidel nähtavast. Kui mul näiteks koguneb 2 2-voldist elementi, on aku väljundis ainult 4 volti. Mitusada kg kaaluva auto liikuma panemiseks kujutage ette, kui palju rakke on vaja ...
Mis toimub prügilas?
Paremal on liitiumi aatomid. Need on esitatud üksikasjalikult, kollane süda tähistab prootoneid ja roheline süda elektrone, mille ümber nad tiirlevad.
Kui aku on täielikult laetud, on kõik liitiumi aatomid anoodi (-) poolel. Need aatomid koosnevad tuumast (koosneb mitmest prootonist), mille positiivne elektrijõud on 3, ja elektronidest, mille negatiivne elektrijõud on 3 (kokku 1, sest 3 X 3 = 1). ... Seetõttu on aatom stabiilne 3 positiivse ja 3 negatiivsega (ta ei tõmba ega tõrju elektrone).
Eraldame liitiumist elektroni, mis osutub ainult kahega: siis tõmbab see + külge ja läbib vaheseina.
Kui ma võtan kontakti + ja - klemmide vahel (nii kui ma kasutan akut), liiguvad elektronid aku välist elektrijuhet mööda - klemmilt + klemmile. Need elektronid pärinevad aga liitiumi aatomite "juustest"! Põhimõtteliselt on 3-st ringi pöörlevast elektronist 1 rebitud ja aatomist jääb alles 2. Ühtäkki ei ole selle elektrijõud enam tasakaalus, mis põhjustab ka keemilise reaktsiooni. Pange tähele ka seda, et liitiumi aatom muutub liitiumioon + sest nüüd on see positiivne (3 - 2 = 1 / Tuum on väärt 3 ja elektronid on 2, kuna kaotasime ühe. Liitmine annab 1, mitte 0 nagu varem. Seega pole enam neutraalne).
Tasakaalustamatusest tulenev keemiline reaktsioon (pärast elektronide purustamist voolu saamiseks) põhjustab saatmise liitiumioon + katoodile (klemm +) läbi seina, mis on mõeldud kõike isoleerima. Lõpuks satuvad elektronid ja ioonid + + poolele.
Reaktsiooni lõppedes aku tühjeneb. Nüüd on + ja - klemmide vahel tasakaal, mis takistab nüüd elektrivoolu. Põhimõtteliselt on põhimõte tekitada depressiooni keemilisel/elektrilisel tasemel, et tekitada elektrivool. Me võime seda mõelda kui jõge, mida rohkem see kaldub, seda olulisem on voolava vee intensiivsus. Teisest küljest, kui jõgi on tasane, siis see enam ei voola, mis tähendab, et aku on tühi.
Kas laadida?
Laadimine seisneb protsessi ümberpööramises, süstides elektrone kindlas suunas - ja eemaldades rohkem imemise teel (see on natuke nagu jõe vee täiendamine, et selle voolu uuesti kasutada). Seega taastatakse akus kõik nii, nagu see oli enne tühjenemist.
Põhimõtteliselt kasutame tühjendamisel keemilist reaktsiooni ja laadimisel tagastame algsed asjad (aga selleks on vaja energiat ja seega ka laadimisjaama).
Kanda?
Liitiumakud kuluvad kiiremini kui vanad head pliiakud, mida meie autodes on sajandeid kasutatud. Elektrolüüdil on kalduvus laguneda, nagu elektroodid (anood ja katood), kuid tuleb arvestada ka sellega, et elektroodidele tekib sade, mis vähendab ioonide ülekandumist ühelt küljelt teisele ... Spetsiaalsed seadmed võimaldab teil taastada kasutatud akusid, tühjendades need erilisel viisil.
Võimalike tsüklite arv (tühjenemine + täislaadimine) on hinnanguliselt umbes 1000-1500, nii et pooltsükliga laadimisel on 50 kuni 100% asemel 0 kuni 100%. KÜTEMINE kahjustab tõsiselt ka liitiumioonakusid, mis kipuvad liiga palju energiat tarbides kuumaks minema.
Vaata ka: Kuidas säästa elektriauto akut?
Mootori võimsus ja aku...
Erinevalt termokaamerast ei mõjuta kütusepaak võimsust. Kui teil on 400 hj mootor, siis 10-liitrine paak ei takista teil 400 hj saamist, isegi kui see on väga lühikest aega ... Elektrisõiduki jaoks pole see sugugi sama! Kui aku ei ole piisavalt võimas, ei saa mootor täisvõimsusel töötada... See on nii mõne mudeli puhul, kus mootorit ei saa kunagi lõpuni ajada (välja arvatud siis, kui omanik askeldab ja lisab suure kaliibri aku!).
Nüüd uurime välja: kuidas ELEKTRIMOOTORI töötab
Kõik kommentaarid ja reaktsioonid
Dernier postitatud kommentaar:
mao (Kuupäev: 2021, 03:03:15)
väga hea töö
Il I. 1 reaktsioon sellele kommentaarile:
- administraator SAIDI HALDJA (2021-03-03 17:03:50): See kommentaar on veelgi parem 😉
(Teie postitus on pärast kinnitamist kommentaari all nähtav)
Kirjuta kommentaar
Kuidas suhtute tootjate deklareeritud tarbimisnäitajatesse?
